Por terapia gênica se
entende a transferência de material genético com o propósito de prevenir
ou curar uma enfermidade qualquer. No caso de
enfermidades genéticas, nas quais um gene está defeituoso ou ausente, a
terapia gênica consiste em transferir a versão funcional do gene para o
organismo portador da doença, de modo a reparar o defeito. Se trata de
uma idéia muito simples, mas como veremos sua realização prática
apresenta vários obstáculos.
Primeira etapa: o isolamento do gene.
Um gene é uma porção de DNA que contém a informação necessária para sintetizar uma proteína.
Transferir um gene é transferir um pedaço particular de DNA. Portanto,
é necessário antes de tudo, possuir “em mãos” o pedaço correto.
As enfermidades genéticas conhecidas estão ao redor de
5000, cada uma causada por uma alteração genética diferente. O primeiro
passo para a terapia gênica é identificar o gene responsável pela
enfermidade. Subsequentemente, pelas técnicas de biologia molecular é
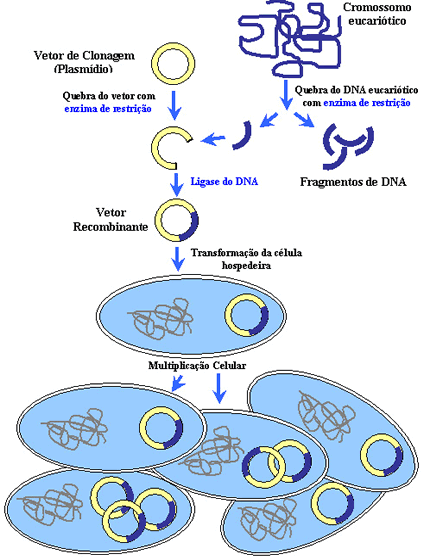
possível adquirir um pedaço de DNA que contém este gene. Esta primeira
etapa é chamada de isolamento ou clonagem do gene.
Qualquer enfermidade é candidata a terapia gênica, desde que o gene esteja isolado para a transferência.
Graças ao progresso da biologia molecular esta primeira
etapa é relativamente simples em comparação a alguns anos atrás. Tem
sido possível isolar numerosos genes causadores de doenças genéticas e,
se descobrem outros a cada semana.
In vivo ou em ex-vivo?
Estas condições mostram qual é o objetivo da transferência gênica. Os procedimentos da terapia gênica in vivo consistem em transferir o DNA diretamente para as células ou para os tecidos do paciente.
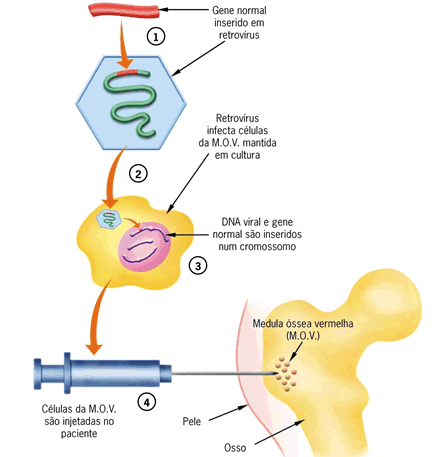
Nos procedimentos ex-vivo, o
DNA é primeiramente transferido para células isoladas de um organismo,
previamente crescidas em laboratório. As células isoladas são assim
modificadas e podem ser introduzidas no paciente. Este método é
indireto e mais demorado, porém oferece a vantagem de uma eficiência
melhor da transferência e a possibilidade de selecionar e ampliar as
células modificadas antes da reintrodução.
Como se transfere o DNA a célula hospedeira?
Os procedimentos de transferência do DNA in vivo ou em ex-vivo
têm o mesmo propósito: o gene deve ser transferido para dentro das
células, e uma vez inserido tem que resistir bastante tempo. Neste
tempo, o gene tem que produzir grandes quantidades de proteína para
reparar o defeito genético. Essas características podem ser resumidas
em um único conceito: o gene estranho precisa se expressar de modo
efetivo no organismo que o receberá.
O sistema mais simples seria, naturalmente, injetar o DNA diretamente nas células ou nos tecidos do organismo a ser tratado.
Na prática, este sistema é extremamente ineficaz: o DNA desnudo quase
não apresenta efeito nas células. Além disso, essa tentativa requer a
injeção em uma única célula ou grupos de células do paciente.
Por isto, quase todas as técnicas atuais para a transferência de material genético implicam o uso de vetores, para transportar o DNA para as células hospedeiras.
Os vetores virais
Os vetores virais são vírus manipulados geneticamente,
de modo a reduzir a sua patogenicidade, sem anular totalmente o seu
poder de infectar as células do hospedeiro (leia mais sobre isso no
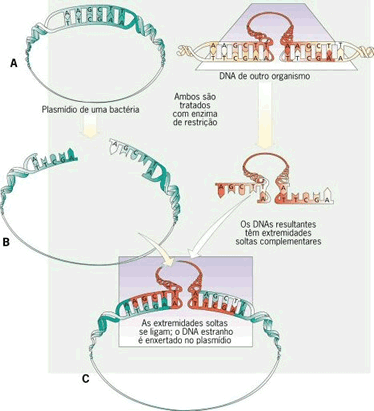
conteúdo de vírus) Com as técnicas da engenharia genética é possível
somar ao DNA do vírus o gene que se quer transferir a determinada
célula. Deste modo, o vírus infectando a célula, trará consigo uma ou
mais cópias do gene desejado.
- Os retrovírus
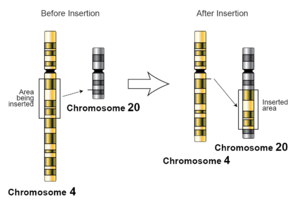
possuem a habilidade de integrar o seu DNA dentro dos cromossomos da
célula infectada. Então, o gene será inserido no genoma das células
hospedeiras e, podem assim ser transmitidos a todas as células-filhas
das infectadas. Eles infectam somente as células que estão
proliferando.
- Os lentivírus,
como o HIV, permitem também transferir material genético para células
que não proliferam (como os neurônios e células do fígado) ou para
células refratárias para o retrovírus (como as células retiradas da
medula óssea).
- Os adenoassociados
de vírus também integram o seu DNA ao cromossomo da célula hospedeira.
Eles têm a vantagem de serem inofensivos para a natureza em relação ao
retrovírus, mas não são capazes de transportar genes de dimensões
grandes.
- Os adenovírus
não são capazes de integrar o seu DNA ao cromossomo da célula
hospedeira. Eles podem transportar genes de grandes dimensões, mas a
expressão deles não dura muito tempo.
Os vetores não virais
Os lipossomos
são essencialmente os únicos vetores não virais utilizados
freqüentemente. As esferas de lipídeos podem ser um importante meio
para a transferência gênica. Em comparação aos vírus, eles têm a
vantagem de não introduzir algum risco em condições de segurança, mas
eles não possuem grande eficiência e são muito seletivos. Os limites da terapia gênica
As principais dificuldades enfrentadas por pesquisadores que lidam com terapia gênica são as seguintes:
A eficiência da transferência
Um especialista em terapia gênica uma
vez afirmou: “a terapia gênica” sofre de três problemas técnicos
principais; a transferência, a transferência e a transferência”.
Nos estudos de terapia gênica, a maior parte dos esforços é
concentrada na procura de vetores que possam transferir o DNA de modo
eficiente, principalmente para células desejadas. Nestes últimos anos
foram inventados e testados uma grande variedade de vetores, alguns dos
quais com chances de expressar o gene estranho em um tipo celular
específico (como glóbulos brancos, células do músculo, das vias
respiratórias, etc.). Alguns destes estão em vias de experimentação no
homem e, a esperança é que apareçam resultados bons.
A duração da expressão
A terapia gênica é praticamente inútil se a expressão do
gene estranho não é mantida por um bom período de tempo. As pesquisas
estão orientadas de maneira a desenvolver sistemas que apresentem uma expressão duradoura, de modo a submeter o paciente a um único tratamento, ou a tratamentos repetidos em períodos maiores (anos).
A segurança do procedimento
Este é um problema particularmente evidente para os vetores virais. Alguns destes derivam de vírus perigosos
como o HIV. É então necessário que antes do uso destes vetores sejam
submetidos a critérios de segurança, particularmente no que concerne a
presença de genes que podem determinar a patogenicidade do vírus
utilizado para infectar (transferir o gene desejado) para as células do
hospedeiro.
A reação imunitária
Como toda substância estranha, o produto do gene novo, o
gene propriamente dito ou seu vetor podem instigar uma resposta
imunitária no organismo sob tratamento. Isto pode causar a eliminação
das células modificadas geneticamente, ou a inativação da proteína
produzida pelo gene novo. No desenvolvimento de estratégias novas de
terapia gênica procura-se evitar respostas imunitárias ao vetor ou ao
produto do gene introduzido. Se trata de uma tarefa difícil e
freqüentemente empírica, mas isso é cada vez mais usado em inovações no
campo da imunologia.
Primeiros resultados
Uma primeira tentativa foi realizada na cura da Síndrome da Imunodeficiência Severa em recém-nascidos, doença provocada pela ausência da enzima adenosina deaminase, o que provoca falhas na resposta imunitária, conduzindo à morte. O gene que codifica para essa enzima foi clonado e injetado com sucesso em leucócitos retirados de crianças afetadas. Em seguida, essas células brancas foram reinjetadas no organismo das crianças. Os resultados são encorajadores, esbarrando, porém, em uma particularidade – glóbulos brancos possuem vida curta e, por esse motivo, a terapia gênica precisa ser constantemente repetida.
Terapia gênica é uma das esperanças dos cientistas em termos de cura e/ou tratamento para a AIDS, doença que , a exemplo da citada acima, incide no sistema imunitário dos pacientes afetados.
Um exemplo de sucesso
Cientistas americanos dizem estar mais próximos da cura do daltonismo usando terapia genética, de acordo com um estudo divulgado na revista científica "Nature" (09/2009).
A equipe das Universidades de Washington e da Flórida conseguiu reparar a capacidade de perceber cores em macacos- de-cheiro (Saimiri sciureus) adultos.
A espécie já nasce sem a habilidade
de distinguir entre o vermelho e o verde porque a visão total depende
de duas versões de um gene chamado opsina, carregado no cromossomo X - uma versão traz o fotorreceptor sensível ao vermelho e a outra ao verde. Como os macacos-de-cheiro machos nascem com apenas um cromossomo X, são daltônicos e incapazes de distinguir entre as duas cores.
A equipe comandada pelo professor Jay Neitz conseguiu introduzir o gene da opsina humano que detecta a cor vermelha nas células receptoras de luz atrás da córnea de macacos adultos.
Para testar a eficiência da terapia genética, os cientistas testaram os macacos Dalton e Sam. Durante o teste, os
animais tinham que identificar as cores em imagens computadorizadas e
recebiam um prêmio - um copo de suco - quando acertavam.
Os resultados indicam que o tratamento foi bem-sucedido. Os macacos que se submeteram ao processo possuem os fotopigmentos necessários para ver todas as cores e foram capazes de distinguir o verde e o vermelho.
Segundo Neitz, as melhorias conquistadas pelo tratamento realizado há dois anos permanecem estáveis, mas os cientistas continuarão monitorando os efeitos do tratamento para avaliar o impacto a longo prazo.
Humanos
Embora ainda sejam necessários mais estudos, Neitz acredita que os resultados oferecem uma perspectiva positiva de que o mesmo tratamento possa ser aplicado em humanos daltônicos.
Até agora, cientistas acreditavam que não seria possível manipular o cérebro de adultos desta forma.
Acreditava-se que acrescentar receptores visuais necessários para uma visão perfeita poderia ser feito apenas nos primeiros anos de vida quando o cérebro ainda é considerado mais maleável.
Winfried Amoaku, especialista em oftalmologia da
Universidade de Nottingham, na Inglaterra, acredita que a pesquisa possa eventualmente beneficiar cerca de 7% dos homens e 1% das mulheres nascidas com deficiência genética na visualização das cores.